Em março, a pasta teve pedido negado para importar a vacina indiana Covaxin; o imunizante teve 80.6% de eficácia em estudo fase 3.
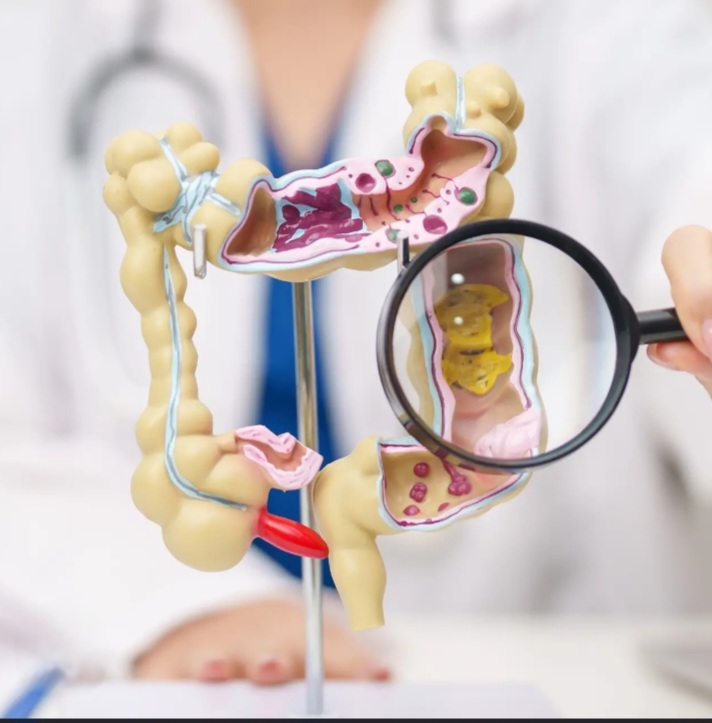
O Ministério da Saúde fará um novo pedido à Agência Nacional de Vigilância Sanitária (Anvisa) de autorização para importar a vacina indiana Covaxin. Em estudo fase 3 divulgado em março, o imunizante demonstrou 80,6% de eficácia na prevenção de casos sintomáticos da Covid-19.
A expectativa da pasta é que, desta vez, a autorização emergencial seja concedida pelo órgão, o que permitirá trazer ao Brasil as 20 milhões de doses já compradas do imunizante ainda neste mês.
No dia 31 de março, a Anvisa rejeitou pedido semelhante do Ministério da Saúde de autorização “excepcional e temporária” para importação e distribuição da vacina Covaxin, imunizante produzido pelo laboratório Bharat Biotech, da Índia.
Na época da recusa, a agência afirmou que os dados apresentados sobre a vacina não comprovaram a “qualidade e eficácia” do imunizante. No dia anterior, a agência já havia indeferido o pedido de certificação das fábricas do laboratório Bharat Biotech.
Os diretores reforçaram que a equipe da Anvisa enviada à Índia identificou inconformidades no processo de fabricação e que, pelos dados apresentados, aceitar a Covaxin naquele momento seria um risco. A avaliação no governo brasileiro seria a de que o quadro mudou em relação à vacina e que os problemas apontados pela Anvisa foram superados e o imunizante já poderia ser aprovado.
O argumento é reforçado pelo fato de que no dia 13/05 a própria Anvisa autorizou os estudos da fase 3 – a última antes da autorização para uso – com 4,5 mil pessoas no Brasil. Os testes estão sendo conduzidos pelo Hospital Albert Einstein, de São Paulo.
Se a aprovação da Anvisa sair em até uma semana, o laboratório indiano indicou que poderá mandar as 20 milhões de doses contratadas até o fim de maio, em duas cargas de 10 milhões de unidades cada. (Com informações da Agência Estado).
Fonte: Metrópoles